
第一作者:卢涵婧,黎敏
通讯作者:刘笑然、李景华、骆丁
通讯单位:海南医科大学第一附属医院
近期,海南医科大学第一附属医院博士研究生卢涵靖在纳米生物医学领域权威期刊Journal of Nanobiotechnology(中科院一区,IF:12.6)发表了题为《NIR-responsive prussian Blue/Fer-1 co-loaded nanozymes for synergistic therapy of acute lung injury》的原创研究成果。该研究成功构建雾化吸入式近红外(NIR)响应型普鲁士蓝/铁抑素-1(Fer-1@PB)共载纳米酶,系统验证了其在脓毒症相关急性肺损伤(ALI)中的靶向治疗效果,并首次揭示CXCL2/ARF6/NCF1信号轴介导的核心分子调控机制,为ALI的精准纳米治疗提供了新的方案。
脓毒症相关ALI是临床常见急危重症,炎症风暴与氧化应激级联反应、铁死亡过度激活共同构成其复杂病理网络,临床缺乏靶向性强、安全性高的药物治疗手段,且传统全身给药存在肺组织富集效率低、系统毒副作用大等瓶颈。针对上述临床痛点,研究团队设计并合成了兼具多酶模拟活性与铁死亡抑制功能的Fer-1@PB纳米酶,采用雾化吸入给药方式实现肺部直接靶向递送,依托普鲁士蓝的NIR光控释药特性与适宜的理化性质(粒径约165 nm、表面负电位)实现高效肺滞留。经ICP-MS体内药代与分布定量证实,该纳米酶主要在肺组织富集代谢,肝肾蓄积极少,具备良好的生物安全性。体内外实验结果显示,Fer-1@PB可通过普鲁士蓝的SOD、CAT等多酶模拟活性高效清除ROS,同时借助Fer-1直接阻断脂质过氧化链式反应抑制铁死亡,二者协同发挥抗炎、抗氧化作用,显著降低TNF-α、IL-6、IL-1β等炎症因子水平,改善肺组织病理损伤、降低肺湿干比并提升FVC、IC等核心肺功能指标,有效提高ALI模型大鼠存活率。
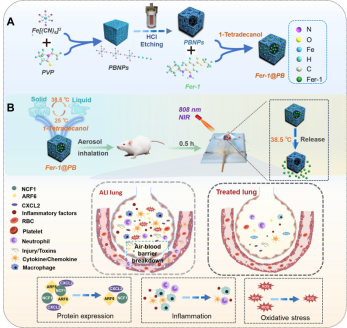
机制研究方面,团队通过转录组学筛选核心差异基因,经qRT-PCR、Western Blot、免疫荧光等技术验证,明确Fer-1@PB通过调控CXCL2/ARF6/NCF1信号轴发挥肺保护作用;同时补充GPX4、ACSL4、4-HNE、Fe²+等铁死亡关键标志物检测,夯实了其体外铁死亡抑制的直接证据,且通过NIR照射对比实验验证了治疗功率密度的生物安全性。
该研究以临床急危重症需求为导向,构建了“靶向递送-协同治疗-机制解析”的完整研究体系,不仅为ALI提供了安全高效的纳米治疗新策略,也为氧化应激与炎症相关肺部疾病的纳米药物研发提供了新思路。
据悉,该研究依托教育部急救与创伤重点实验室、海南省创伤与灾难救援重点实验室平台完成,是我院研究团队长期聚焦急危重症领域,围绕急慢性肺损伤治疗、多模态调控及分子机制开展系统性研究的重要成果。该团队相关研究已陆续发表于《Communications Biology》《Chemical Engineering Journal》等国际权威期刊,获得国家自然科学基金项目、科技部重大专项子课题、海南省重点发展项目等多项资金支持,为急危重症精准诊疗与临床转化奠定了坚实基础。